学术前沿 | 帕金森病疼痛的诊断、分类与治疗进展
来自:学术前沿 日期:2026-03-06 10:10
在全球范围内,帕金森病(PD)是增长最快的神经系统疾病,患者人数超过千万。然而,常常被运动症状所掩盖的是另一个高发的“隐形杀手”——慢性疼痛,它困扰着超过三分之二的帕金森病患者,严重侵蚀着他们的日常生活质量。
长期以来,帕金森病疼痛的诊断和治疗缺乏标准化框架,导致其评估不足、管理不佳。2021年,国际专家团队推出了帕金森病疼痛分类系统(PD-PCS),为这一困境带来了革命性的解决方案。
一、为何需要新的分类系统? 帕金森病疼痛的复杂性与挑战
帕金森病疼痛并非单一实体,其临床表现千差万别。传统的分类方法存在明显局限: 机制不明:缺乏基于病理生理学的分类框架。 覆盖不全:忽略了与帕金森病不相关的疼痛以及伤害可塑性疼痛(Nociplastic Pain)。 验证不足:部分系统未经过严格验证。 PD-PCS系统应运而生,它旨在解决三大核心挑战: 因缺乏标准化分类工具导致的疼痛漏报和评估不足。 未能充分利用标准区分PD相关疼痛与其他原因疼痛。 众多非运动症状与疼痛双向加重的复杂局面。
二、PD-PCS的核心: 两步法精准分类
PD-PCS系统通过清晰的逻辑流程进行分类,其核心在于两步走策略: 第一步:界定疼痛与帕金森病的关联性 慢性疼痛首先被划分为与PD相关或与PD无关。 诊断为PD相关疼痛,需满足以下至少一项标准: 疼痛出现与PD发病同时发生 PD发病后疼痛加重 疼痛出现在药物“关”期(低多巴胺能刺激) 疼痛对多巴胺能治疗有反应 疼痛出现在相对多巴胺能过度刺激时(如药物峰剂量舞蹈样运动障碍) 第二步:基于病理生理学机制进行分型 PD相关疼痛进一步分为三大类,这与国际疼痛研究协会(IASP)的分类框架一致: 1 伤害感受性疼痛 (Nociceptive Pain, 55%) 机制:源于非神经组织(如肌肉、关节)的损伤或炎症,导致伤害感受器持续激活。 常见类型:肌肉骨骼疼痛、肌筋膜疼痛综合征、与直立性低血压相关的衣架样头痛。 特点:常对左旋多巴补充治疗有反应。 2 神经病理性疼痛 (Neuropathic Pain, 16%) 机制:由躯体感觉神经系统的病变或功能障碍引起。 常见类型:神经根病变、周围神经病变。 诊断:可根据临床检查和辅助检查(如神经传导研究)分为可能、很可能和确定。 3 伤害可塑性疼痛 (Nociplastic Pain, 22%) 机制:这是PD-PCS强调的新概念。其核心是中枢神经系统对痛觉处理的异常增益,而无明确的组织或神经损伤。 重要提示:文献强调,以往PD中常被模糊地称为“中枢性疼痛”的类型,实质上多属于伤害可塑性疼痛,应与“中枢神经病理性疼痛”严格区分,以避免混淆。 常见类型:腿部运动不宁、非运动“关”期疼痛、多巴胺激动剂戒断综合征相关的疼痛。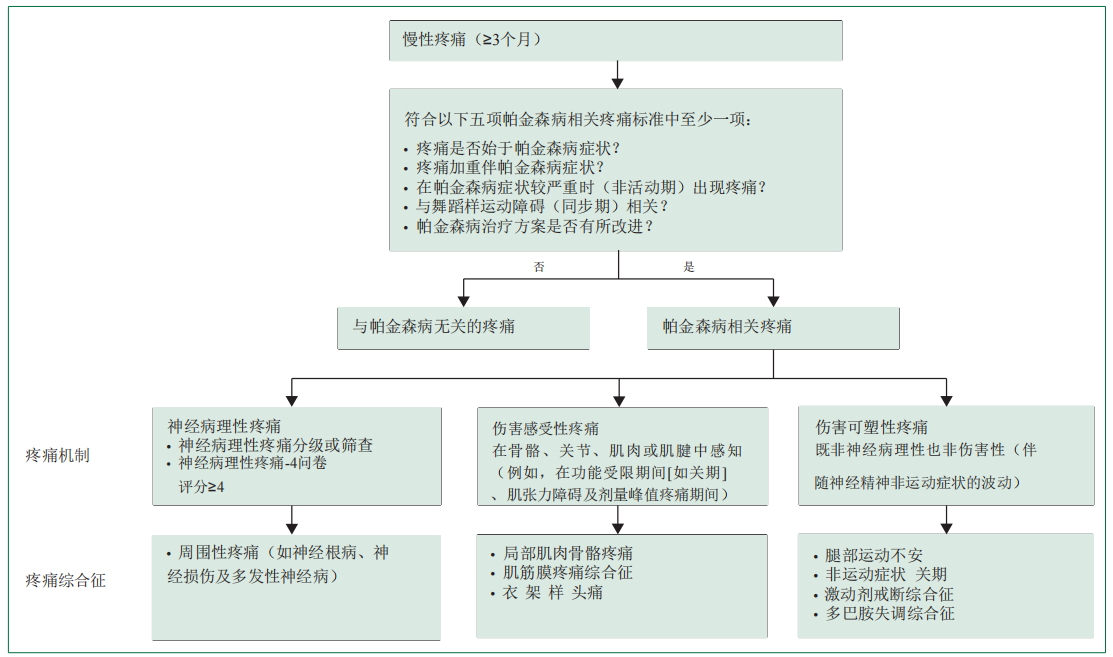
三、从分类到治疗: PD-PCS指导下的管理策略
基于PD-PCS的分类,治疗策略应遵循机制导向的路径。下图展示了一个可能的治疗策略: 1 药物治疗 首要步骤:优化多巴胺能治疗是基础。调整左旋多巴用药方案、添加COMT抑制剂(如恩他卡朋、奥匹卡朋)或MAO-B抑制剂(如沙芬酰胺)以平稳血药浓度,对改善“关”期疼痛尤其重要。 伤害感受性疼痛:除多巴胺能药物外,A型肉毒毒素对局灶性肌张力障碍相关疼痛有效。阿片类药物(如奥施康定-纳洛酮)在部分研究中显示对肌肉骨骼痛和夜间痛有潜在益处,但需权衡风险。 伤害可塑性疼痛:证据有限。一项研究(OXYDOPA试验)显示增加左旋多巴或奥施康定均无效。5-羟色胺和去甲肾上腺素再摄取抑制剂(SNRI,如度洛西汀)在小型研究中显示前景,但需更多证据。值得注意的是,针对后上岛叶的重复经颅磁刺激(rTMS)被证明仅对伤害感受性疼痛有效,这凸显了精准分型对选择非药物疗法同样至关重要。 2 非药物治疗 非侵入性神经调控:rTMS(针对初级运动皮层或岛叶)、经颅直流电刺激(tDCS)等显示出缓解疼痛的潜力。 运动疗法:步行、健走、瑜伽等物理活动被证实能有效减轻疼痛,尤其是腰背痛。 侵入性神经调控:如脑深部电刺激(deep brain stimulation,DBS)、脊髓电刺激(spinal cord stimulation,SCS)。DBS是在脑内核团或特定脑区植入刺激电极,通过脉冲电刺激调控相关核团或脑区的功能,不仅能改善运动症状,对疼痛(尤其是肌张力障碍性和肌肉骨骼痛)也有长期积极作用。SCS是将电极置入椎管硬膜外腔,通过植入体内的刺激器发出电脉冲信号,刺激脊髓背柱来调节神经系统功能达到缓解疼痛的目的,并且研究表明对帕金森病伴随的运动障碍也有一定改善作用。 脑深部电刺激,尤其是丘脑底核DBS(STN-DBS)对疼痛的治疗效果已在几项非随机研究中进行了评估。大多数已发表的研究报告了超过6个月的积极效果,其中一项研究显示效果可持续长达8年。“一项涉及41名有难治性运动症状的帕金森病患者的研究显示,STN-DBS对肌张力障碍和肌肉骨骼疼痛有积极作用,但对中枢性或神经性病理性疼痛没有积极作用,这是通过手术后1年疼痛患病率和强度的变化来衡量的。然而,这种治疗的改善似乎与运动改善和情绪变化无关。Oswestry腰痛功能障碍指数的改善评分用于评估腰痛引起的残疾和功能损害程度,在16名腰痛患者中,双侧STN-DBS治疗后至少1年内仍然有效。”一项开放标签随机对照试验(RCT)比较了苍白球内侧部深部脑刺激(DBS)与丘脑底核-DBS(STN-DBS)的疗效,结果显示在27例患者中,STN-DBS组在非运动症状量表(NMS)感觉主诉分项(表)评估的疼痛相关结局方面显示出更显著的改善。一项短期、随机、双盲、对照交叉研究比较了STN-DBS在开启状态与关闭状态下的效果,研究对象为16名伴有或不伴有神经病理性疼痛的帕金森病患者。研究结果显示,开启状态通过基于Peltier的接触温度刺激装置评估,可提高主观热痛阈值;同时通过 H₂¹⁵O PET测量,可降低痛觉诱发的体感皮层脑活动。 脊髓电刺激(SCS)对帕金森病患者运动与非运动功能结局的影响尚存争议,因现有研究报道结果不一。2023年一项系统评价纳入了5项非随机研究,共56例伴有下背部或下肢疼痛的帕金森病患者,多数研究显示出积极疗效,疼痛强度平均减轻59%。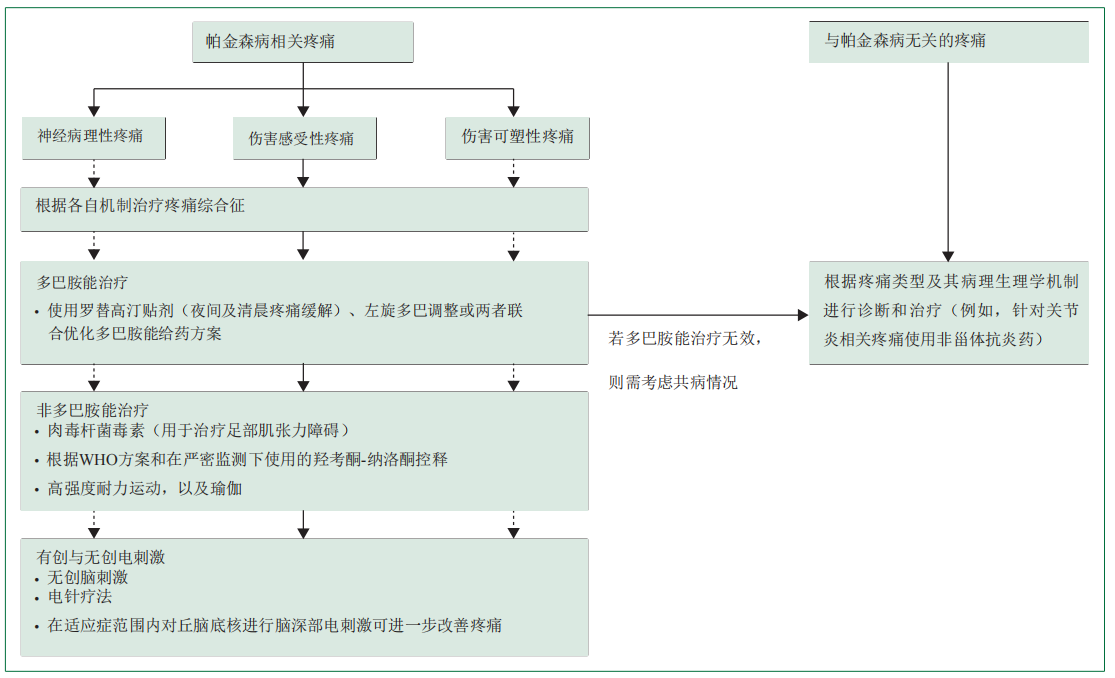
四、疼痛背后的科学: 多因素交织的病理生理学
帕金森病疼痛的机制复杂,涉及多水平神经系统功能障碍: 中枢机制:多巴胺能系统是关键因素。基底节区通过多巴胺传递整合痛觉感知。此外,去甲肾上腺素能、5-羟色胺能、谷氨酸能等非多巴胺能通路也深度参与。 周围机制:α-突触核蛋白病理可能影响周围神经,导致小纤维损伤,参与神经病理性疼痛。 感觉处理异常:研究发现,PD患者存在普遍的痛觉阈值降低(痛觉过敏),且左旋多巴仅能逆转部分这种异常,提示非多巴胺能机制的重要作用。 心理社会因素:焦虑、抑郁与疼痛形成恶性循环,强调了生物-心理-社会综合管理模式的重要性。 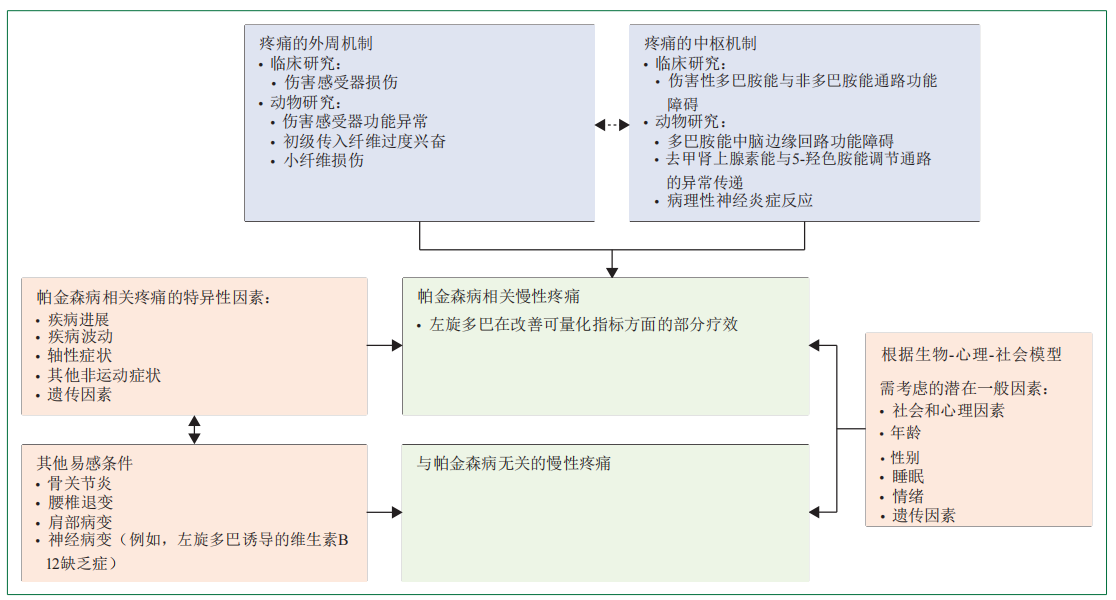
五、总结与展望: 迈向精准疼痛医学的未来
PD-PCS系统为帕金森病疼痛的标准化诊断和机制导向治疗奠定了坚实基础。通过准确识别疼痛类型,临床医生可以: 更有效地制定个体化治疗方案。 更精准地设计临床研究,针对特定疼痛类型进行干预。 最终显著改善患者的生存质量。 未来,需要更多设计严谨、以疼痛为主要终点的随机对照试验,并遵循临床实验的研究方法、监测及疼痛评估倡议,结合帕金森病亚型分型和先进的影像学生物标志物,有望真正实现帕金森病疼痛的精准医疗。
参考文献: Tinazzi M, Gandolfi M, Artusi CA, Bannister K, Rukavina K, Brefel-Courbon C, de Andrade DC, Perez-Lloret S, Mylius V. Advances in diagnosis, classification, and management of pain in Parkinson's disease. Lancet Neurol. 2025 Apr;24(4):331-347. doi: 10.1016/S1474-4422(25)00033-X. PMID: 40120617.