学术前沿 | 丘脑底核自适应刺激与传统深部脑刺激治疗帕金森病的疗效对比:一项多中心回顾性研究
来自:学术前沿 日期:2025-06-16 09:37
近日,Neuromodulation期刊(Q2,中科院二区,IF=3.2)在线发表了由首都医科大学宣武医院牵头,浙江大学医学院附属第二医院、中国科学技术大学附属第一医院、山东大学齐鲁医院、徐州医科大学附属医院、首都医科大学三博脑科医院、武汉大学人民医院、天津市环湖医院多家中心共同参与的题为 “Adaptive vs Conventional Deep Brain Stimulation of the Subthalamic Nucleus for Treatment of Parkinson's Disease: A Multicenter Retrospective Study”的研究成果。
作者团队
Qinghua Li(李庆华),Kailiang Wang(王开亮),Jiping Li(李继平),Penghu Wei(魏鹏虎),Yongzhi Shan(单永治),Jianyu Li(李建宇),Junming Zhu(朱君明),Zhe Zheng(郑喆),Chaoshi Niu(牛朝诗),Chi Xiong(熊赤),Weiguo Li(李卫国),Qianqian Wu(吴倩倩),Qihua Xiao(肖其华),Guiyun Cui(崔桂云),Xiongfei Wang(王雄飞),Yuguang Guan(关宇光),Guoming Luan(栾国明),Baohui Liu(刘宝辉),Huimin Dong(董慧敏),Siquan Liang(梁思泉),Haitao Li(李海涛),Wenwen Xu(徐文文),Guoguang Zhao(赵国光),Yuqing Zhang(张宇清)
该研究通过多中心临床试验,评估了国产新型自适应闭环神经调控系统(CNS)治疗帕金森病(PD)为期一年的安全性与有效性,核心目标为对比自适应脑深部电刺激(aDBS)与传统脑深部电刺激术(cDBS)的疗效差异。
本回顾性研究纳入62例行双侧丘脑底核(STN)DBS治疗的PD患者。采用国际运动障碍学会帕金森病综合评价量表(MDS-UPDRS)、帕金森病生活质量量表(PDQ-39)、Schwab-England生活功能量表评估疗效,并监测左旋多巴等效日剂量(LEDD)变化及不良事件。试验设计分为两阶段:术后90天将患者随机分组进行刺激开启组(Stim-on)与刺激关闭组(Stim-off)对照研究,术后360天进行非随机化aDBS与cDBS疗效对比。
结果:术后90天数据显示,除药物开期状态下的LEDD及语言功能外,Stim-on组各项指标均显著优于Stim-off组。术后360天评估中,aDBS组在关键指标上展现出显著优势:
MDS-UPDRS II评分改善率(57.29% vs 33.02%, p=0.022);
MDS-UPDRS IV评分改善率(59.83% vs 36.69%, p=0.026);
PDQ-39生活质量提升率(56.91% vs 27.37%, p=0.031);
LEDD降低幅度(53.35% vs 29.16%, p=0.002);
CNS-aDBS系统成功捕获清晰的STN-β振荡信号,该信号具备成为疗效生物标志物的潜力。
引言
帕金森病(Parkinson’s disease, PD)是第二大与衰老相关的神经退行性疾病。随着人类寿命延长,PD发病率持续攀升,对患者、家庭及社会造成显著负担。以丘脑底核(subthalamic nucleus, STN)或苍白球内侧部(globus pallidus internus, GPi)为靶点的传统脑深部电刺激术(conventional deep brain stimulation, cDBS),数十年来已成为中晚期PD的标准疗法。尽管短期与长期研究均证实cDBS能有效改善PD运动及非运动症状,但其临床应用仍受限于刺激相关副作用(如构音障碍、步态异常)以及频繁调整刺激参数的需求。
近年来,自适应脑深部电刺激(adaptive DBS, aDBS)技术取得重大进展。该技术通过自动调节刺激参数以适应PD患者波动的临床状态,从而提供个体化治疗。过去数十年中,研究者致力于识别临床环境下局部场电位(local field potentials, LFPs)的生理标志物,以支持闭环刺激。其中,β振荡(13–35 Hz)与PD运动症状的关联性因其与病理生理机制的紧密联系,已成为多个研究团队公认的稳健生物标志物。
针对STN区β振荡的检测与响应方法已在PD患者中长期验证。早期研究利用STN区升高的β活动作为生物标志物,触发固定参数的DBS治疗。此外,γ振荡、高频振荡及传感器记录等其他症状特异性标志物也被探索用于评估多标志物组合的疗效。目前多项植入式aDBS设备正进行临床验证:美敦力(Medtronic)推出的初代传感型aDBS设备(Activa™ PC + S)及其升级版(Activa™ RC + S)最初仅限少数临床研究中心使用;2020年首款商用aDBS设备(Medtronic Percept™ PC)上市,其可充电版本(Medtronic Percept™ RC)于2024年推出;除美敦力外,Newronika、波士顿科学(Boston Scientific)、Bioinduction及Neuralink等公司也在持续推进aDBS技术优化。
既往研究已证实基于β振荡的aDBS较cDBS更具疗效优势且副作用更少。本项回顾性多中心研究旨在评估一种新型可充电DBS设备,该设备提供aDBS与cDBS双模式刺激:其植入式脉冲发生器(implantable pulse generator, IPG)可通过电极实时记录靶核团LFP信号,并经由嵌入式闭环算法处理数据以动态调节刺激参数,同时将刺激器的数据无线传输到记录设备进行进一步的实时分析。aDBS反馈刺激是在收集的β振荡的基础上进行的。研究者通过为期一年的随访观察,采用标准化临床症状量表系统比较两种模式的疗效差异。
患者分组和干预方案
回顾性分析了来自8个临床中心的62例PD患者的数据,比较了aDBS和cDBS的结果。如图1所示,所有患者被随机分为刺激开启组(n = 32)和刺激关闭组(n = 30)。刺激开启组,术后20±15天开始启动cDBS治疗,而刺激关闭组在术后90天开始接受DBS治疗。术后90-180天,根据患者意愿及β振荡信号监测可行性,将患者分为aDBS组(n = 30)和cDBS组(n = 32)。只有表现出可检测到的β带和耐受aDBS的患者被纳入aDBS组。这两组患者均匀分布在各参与中心。从手术后180至360天,所有患者延续此前分配的模式(aDBS或cDBS)持续治疗至术后360天。
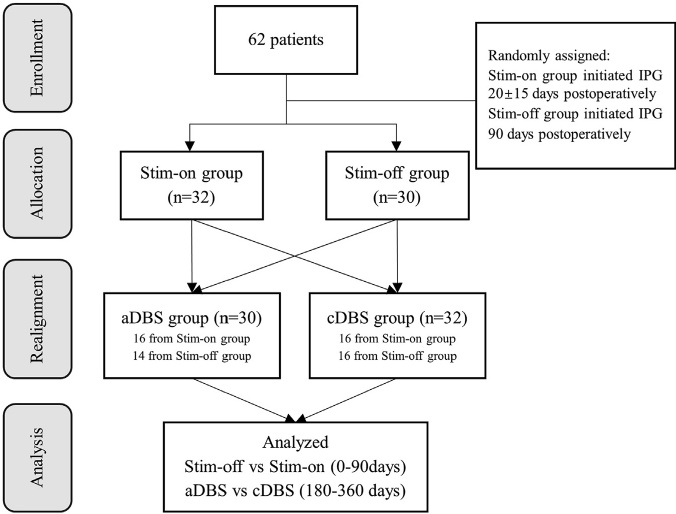
图1 CNS临床试验流程图
临床特征评估涵盖性别、确诊年龄、病程、MDS-UPDRS、汉密尔顿抑郁量表、PDQ-39(帕金森病生活质量问卷)、左旋多巴等效日剂量(LEDD)、简易智力状态检查(MMSE)、Schwab-England生活功能量表(SES)。评估时间点:基线、术后90天、术后360天;每次评估均包含药物关期(Med-off)与药物开期(Med-on)双状态。通过记录患者报告的不良事件的严重程度和频率来评估安全性。研究方案经参与中心的机构审查委员会或伦理委员会批准(批准文号[2021]021)。在纳入本研究之前,所有患者均获得了书面知情同意。所有患者还被纳入另一项临床试验研究(ChiCTR2100054906)。
DBS手术采用立体定向框架结合术中微电极记录技术,为患者双侧植入靶向丘脑底核(STN)的电极,以及可充电感知型闭环神经调控系统(CNS)(常州瑞神安医疗器械有限公司)(图2)。基于术前MRI确定靶点坐标。术中将延伸导线连接至可采集局部场电位(LFP)的脉冲发生器。通过术中行为测试确认刺激有效性,规避潜在副作用。结合术前MRI与术后CT影像验证电极触点位置。
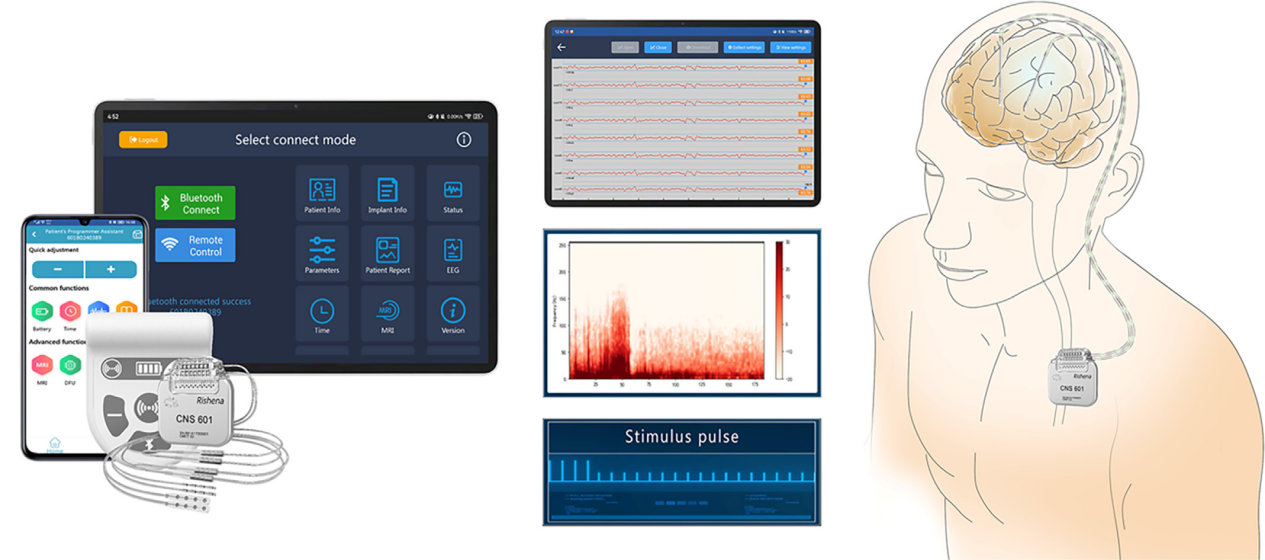
图2
CNS系统包括电极、导线、支持信号记录的可充电植入式脉冲发生器(IPG),以及嵌入手机/平板的移动应用程序。
移动应用界面截图:展示实时局部场电位(LFP)记录与刺激脉冲反馈。
需要特别指出的是,截至本文发表时,该款自适应闭环神经调控系统(CNS),尚未获得主要医疗器械监管机构的上市批准,尚未投入商业应用。
这款用于帕金森病治疗的自适应闭环神经调控系统(CNS)采用创新的数据采集与反馈机制:每5秒进行神经信号采集与分析后,接续54秒的刺激反馈阶段,并设置1秒间歇期以消除刺激伪迹,确保记录信号的精确性。电极通过双极记录方式以250 Hz采样率实时采集局部场电位(LFPs),相邻触点分别作为参考电极和记录电极。原始信号首先经过1 Hz四阶巴特沃斯高通滤波以去除直流成分,再通过50 Hz陷波滤波消除工频干扰。随后,滤波后的信号通过短时傅里叶变换(STFT)转换为时频域,并生成时频图以展示不同频段能量随时间的变化。对信号分段平均后得到功率谱,从时频图中可识别β频段(13-18 Hz)的能量集中区域,例如时频图清晰显示15 Hz的功率谱峰值频率。植入式脉冲发生器的内置闭环算法自动分析采集的LFPs,并发出反馈刺激以抑制病理性升高的β振荡(图3)。
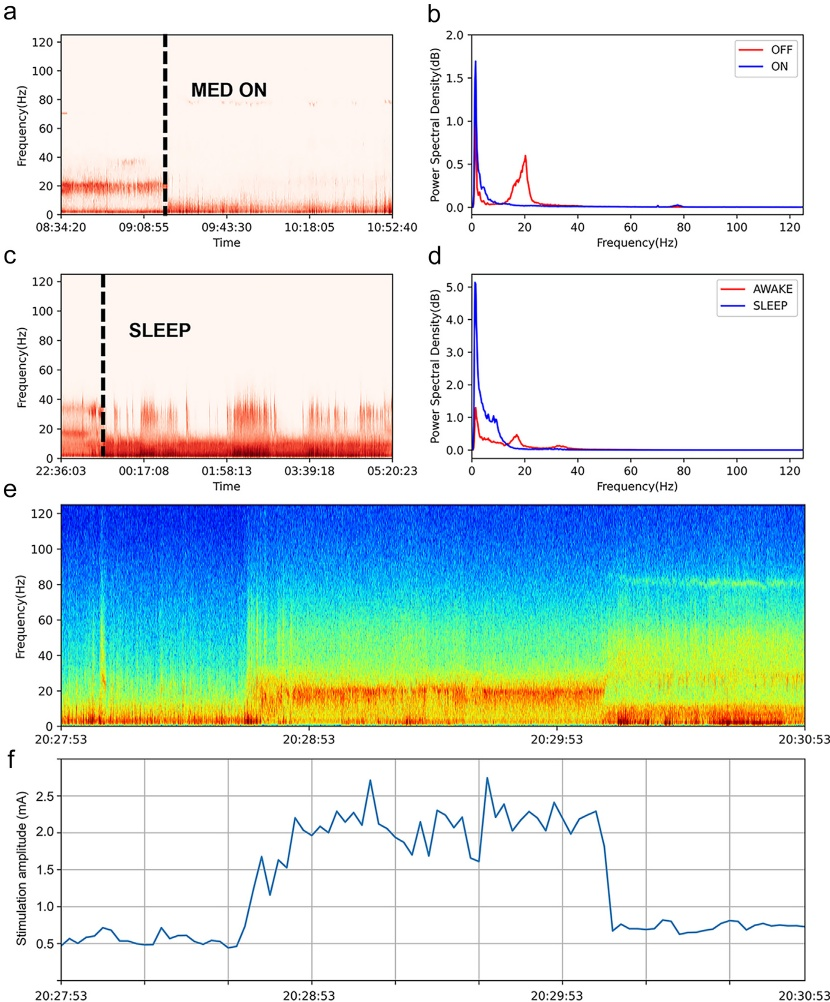
图3
LFP记录与自适应刺激
CNS设备从所有入组患者中成功获取了可监测的LFP变化,并记录了不同状态(包括停药/用药、睡眠/清醒)下STN-LFP(丘脑底核局部场电位)的变化。为便于说明,我们展示了一例植入患者的代表性电生理数据(图3a-d)。
通过实时采集和分析STN-LFP,自适应刺激被应用于异常增强的β振荡,从而抑制β信号并缓解帕金森病(PD)患者的临床症状(图3e-f)。
统计分析
采用卡方检验(χ2检验)评估aDBS组与cDBS组间的性别差异。通过Mann-Whitney U检验比较组间疗效差异,包括Stim-off组与Stim-on组从基线至90天的改善差异,以及aDBS组与cDBS组从基线至360天的改善差异。p<0.05视为具有统计学显著性。数据分析使用IBM SPSS Statistics for Windows(版本27.0;IBM Corporation,Armonk,NY)完成。
结果
本回顾性研究共纳入62例患者(男性34例,女性28例;平均发病年龄50.97±9.78岁;病程8.98±5.41年)。Stim-on组(n=32)与Stim-off组(n=30)、cDBS组(n=32)与aDBS组(n=30)的基线特征具有可比性(表1)。研究期间未观察到显著的中心间差异。
术后90天刺激关闭组与刺激开启组的比较
如表2所示,刺激开启组和刺激关闭组在以下指标中察到显著差异:MDS-UPDRS II(42.37%±33.16% vs -10.97%±65.15%,p<0.001);MDS-UPDRS III(药物关期:48.38%±19.81% vs 5.03%±23.15%,p<0.001;药物开期:27.48%±50.44%vs2.54%±32.51%,p<0.001),MDS-UPDRS IV(42.02%±33.94% vs 4.75±55.64%,p<0.001), PDQ39(35.41±49.77% vs - 9.60±48.10%,p<0.001),SES(20.74%±24.95% vs 10.14%±23.29%,p=0.029)。然而,在LEDD减少方面,两组无统计学差异(24.58%±25.32% vs 12.63%±27.59%,p=0.051)(图4)。
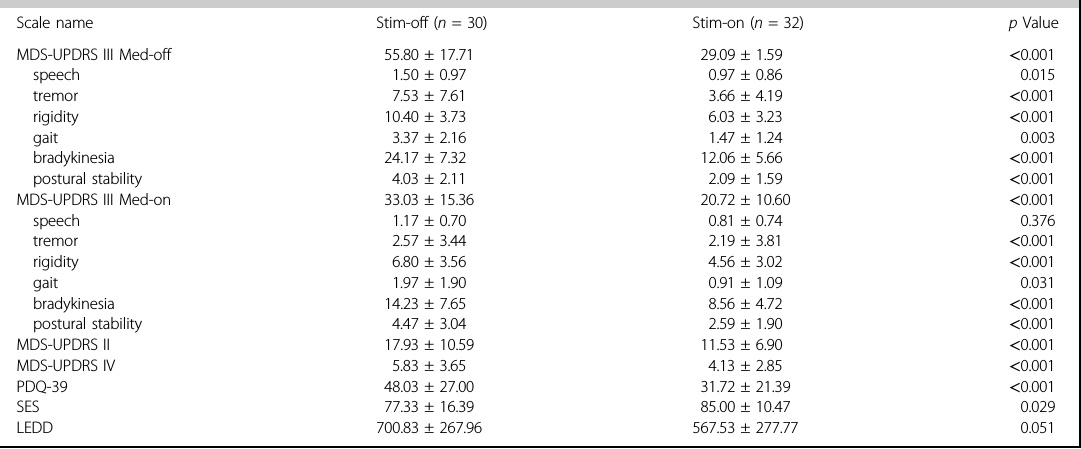
表2
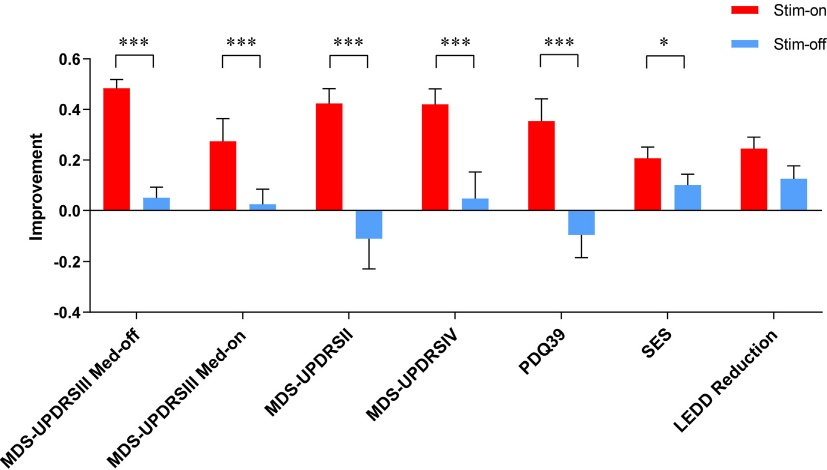
图4
MDS-UPDRS III亚组分析显示,药物开期下两组言语功能改善无显著差异(13.33% ± 69.16% vs 1.39% ± 55.59%,p=0.529),而其他运动亚组(如震颤、强直等)无论药物关期/开期状态,刺激开启组均显著优于刺激关闭组(p<0.05)。
aDBS与cDBS组长期疗效比较
术后360天评估显示,与基线相比,aDBS和cDBS均显著改善帕金森病患者的运动及非运动症状(表3)。但aDBS组在以下指标中表现出统计学优势:MDS-UPDRS II:57.29% ± 26.81% vs 33.02% ± 56.16%(p=0.022);MDS-UPDRS IV:59.83% ± 66.41% vs 36.69% ± 62.61%(p=0.026);PDQ-39:56.91% ± 29.77% vs 27.37% ± 69.94%(p=0.031);LEDD减少率:53.35%± 28.02% vs 29.16% ± 30.63%(p=0.002)(图5)
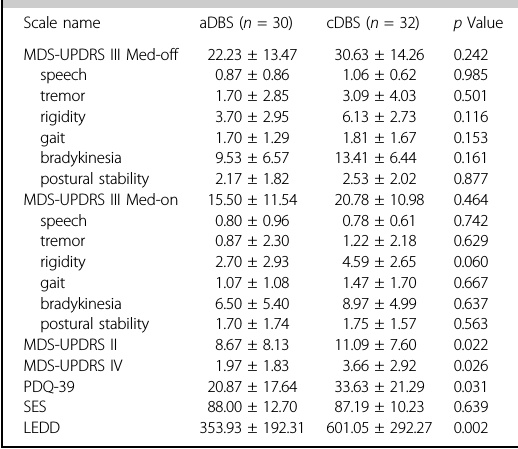
表3
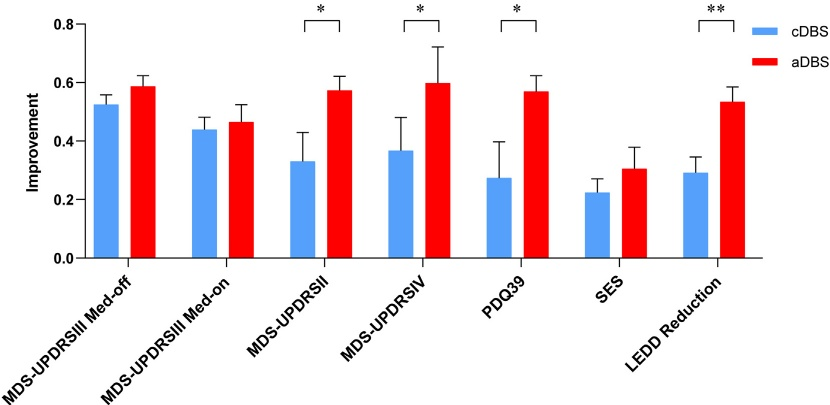
图5
两组在MDS-UPDRS III(运动功能)及其运动亚组评分改善率、以及SES(副作用评分)方面无显著差异(p>0.05)。
不良事件
在为期一年的随访期间共报告17例不良事件(发生率27.42%)和2例严重不良事件(发生率3.23%)。所有17例不良事件均与设备无关,唯一与设备相关的严重不良事件源于植入式脉冲发生器(IPG)软件故障,导致患者在术后三个月无法充电。更换IPG后患者恢复良好并继续参与研究。
讨论
在这项回顾性研究中,对62名帕金森病患者进行了CNS设备的有效性和安全性评估,这些患者来自一个多中心队列,并且有为期一年的随访数据。研究结果证实了CNS设备的治疗有效性,特别是在术后90天内,Stim-on组的临床效果显著优于Stim-off组。文献报道的cDBS长期疗效可使MDS-UPDRS III评分改善28%-71%,与本研究中cDBS治疗组90天改善55.80%、360天改善52.42%的结果接近。本研究第二阶段显示,无论是cDBS还是aDBS,均能显著缓解运动症状并提升生活质量。然而目前关于aDBS长期疗效的研究相对有限。本研究发现,在术后360天通过MDS-UPDRS III评分和SES量表评估,aDBS的疗效与长期cDBS相当。进一步的MDS-UPDRS III亚组分析表明,在停药和用药两种状态下,各治疗组间的评分差异均不显著。
在用药状态下,开机组与关机组在言语改善方面未观察到显著组间差异,LEDD降低率亦无显著差异。这些差异值得从机制和临床角度深入探讨:首先,用药状态下开机组缺乏言语改善,可能反映言语相关神经网络对短期cDBS的调节敏感性有限;亦或是多巴胺能补偿效应掩盖了该特定领域的刺激获益。其次,两组LEDD降低率相当的原因在于标准化临床方案要求推迟激进减药直至术后病情稳定,该时间点恰与关机组开机时间重合。此方案本质上限制了早期多巴胺能依赖性的差异评估,提示90天观察窗后的长期LEDD变化轨迹或能更有效阐明刺激诱导的药物节省效应。
尽管在长期刺激中,aDBS展现出与cDBS相当的运动症状控制能力,但aDBS在MDS-UPDRS II/IV、PDQ39及LEDD降低率方面具有更显著的多维疗效优势,标志着aDBS成为一种更全面的神经调控策略。该结果与既往研究一致:aDBS可能在功能预后、运动并发症改善及药物减量方面提供更优的治疗获益。aDBS组在MDS-UPDRS IV评分的显著改善,部分归因于LEDD的同步降低,从而有效规避左旋多巴诱导并发症的风险。
何等人报道称,aDBS与cDBS在改善运动功能方面疗效相当,无显著差异。一项纵向案例研究显示,aDBS实现了多巴胺能药物完全停用,并减少了治疗相关并发症。值得注意的是,该患者始终倾向选择aDBS,因其能增强运动稳定性并提升日常活动表现[26]。这些发现凸显了aDBS的独特优势,表明其有望为患者特定需求提供更全面的治疗方案。
本研究中,所有患者均植入双侧丘脑底核(STN)电极。中枢神经系统的aDBS模式以STN的β振荡作为反馈刺激的生物标志物:当β信号超过预设阈值时增强刺激,当β信号低于该阈值时减弱刺激。既往研究证实β振荡与帕金森病(PD)症状密切相关,STNβ活动已被广泛认定为aDBS获得良好临床疗效的可靠生物标志物。Little等在晚期PD患者队列中发现,基于单侧STNβ局部场电位(LFP)驱动的aDBS疗效显著,aDBS与cDBS均能明显改善MDS-UPDRS评分,而aDBS在缓解症状和缩短刺激时间方面更具优势。多项研究证实,基底神经节过度的β频段活动是运动症状(尤其是运动迟缓和强直)严重程度的生物标志物[。如图3所示,STNβ振荡显著受药物开启/关闭状态及睡眠/觉醒状态影响。多巴胺能治疗和/或DBS已被证实可抑制β活动,其抑制程度与PD症状改善相关。Mathiopoulou等发现药物主要影响低频β波段,而DBS对高频β波段的抑制更为显著。与此同时,针对STN区β振荡及其他LFP振荡的算法研究持续深入,已提出适用于患者不同状态的单阈值与双阈值模式,以适应不同患者的LFP变异并优化PD刺激参数。
尽管STN的β频段活动并非对所有患者都最优,但其已被广泛采纳为帕金森病aDBS的生物标志物。研究表明,除β振荡外,不同频段的振荡模式可能与运动症状(如震颤、运动迟缓和异动症)及非运动症状(如抑郁和冲动行为)相关。θ/α频段(3-12Hz)与运动症状存在关联;γ活动(31-100Hz)涉及自适应刺激和长期神经记录;而高频振荡(>200Hz)尤其在与β活动耦合时,可为优化STN刺激靶点提供临床依据。尽管取得这些进展,既往研究多受限于样本量小和试验周期短。荟萃分析指出短期研究占主导地位,强调需开展更大规模的LFP记录长期研究。本工作在此领域迈进了一步,未来数年将持续推进。
本研究中CNS系统的aDBS模式与美敦力Percept™ PC/RC系统运行机制不同:CNS设备采用更具结构化的自主循环模式,其独特优势在于设置1秒休止期与5秒采集期,这有助于降低刺激伪迹影响、防止过度刺激并减少副作用。该方法可确保更稳定的刺激输出,降低刺激遗漏或过量的风险。虽然设计引入了一定延迟,但我们在实时反馈与疗效间取得了平衡,确保刺激幅度的调整能有效改善运动症状。不过其风险效益比仍有待深入探究。
7例患者植入了CNS方向性电极(CNL602H)。其运动与非运动症状的缓解程度与传统环状电极相当。方向性电极通过定向刺激提供治疗灵活性,有望优化神经靶向定位。
随访期间未见出血、感染、脑损伤后遗症或刺激相关并发症,这与既往研究指出的DBS手术不良事件发生率较低相符。但出现1例设备故障,需更换植入式脉冲发生器(IPG),该发生率与文献报道的IPG故障率(0.1%~13.8%)一致。尽管发生并发症,患者更换IPG后临床症状显著缓解,随访期间未出现其他不良事件。总体而言,本研究不良事件发生率与既往研究相当,进一步证实了DBS治疗帕金森病的安全性。
结论
总之,aDBS和cDBS均为帕金森病的有效治疗方法,长期来看,两者在缓解运动症状方面效果相当。aDBS在减少LEDD、MDS-UPDRS II、MDS-UPDRS IV和SES方面优于cDBS,这表明aDBS可能提供一种更全面的帕金森病症状管理方法。未来的前瞻性研究需要更大的样本和更长的随访时间来进一步验证这些发现。
备注:
文章中共统计分析了临床试验所有受试者(68例)中的62例,6例没有纳入统计,原因为2例不符合本次临床试验的入组标准被剔除,1例脱落,3例受试者不符合回顾性研究的标准被剔除(非单一使用开环或闭环模式)。
该注册临床试验(ChiCTR2100054906)参与单位/主要研究者:
01 首都医科大学宣武医院/张宇清
04 浙江大学医学院附属第二医院/朱君明
07 武汉大学人民医院/刘宝辉
08 首都医科大学三博脑科医院/王雄飞
09 安徽省立医院/牛朝诗
10 山东大学齐鲁医院/李卫国
11 徐州医科大学附属医院/崔桂云
12 天津市环湖医院/梁思泉